Pathologie - Toxicologie
-
Toxicocinétique - Métabolisme [4]
L’acrylate de méthyle est absorbé quelle que soit la voie d’exposition, distribué dans tout l’organisme et rapidement excrété dans l’urine sous forme de métabolites et dans l’air expiré sous forme de CO2.
Chez l'animal
Absorption
Il n'y a pas d'étude spécifique pour mesurer l'absorption de l'acrylate de méthyle ; cependant, une toxicité aiguë, objectivée par des valeurs de DL50 et CL50, a été observée, ce qui présume une absorption quelle que soit la voie d'exposition.
Distribution
Des autoradiographies, réalisées chez le cobaye avec du 14C]-acrylate de méthyle, ont montré une distribution des molécules radiomarquées :
- 2 heures après exposition par voie orale (0,4 mmoles/kg), dans tous les organes y compris le cerveau ; la clairance est rapide, dans les 16 heures suivantes les molécules radiomarquées persistent dans le foie et la vessie. Après 16 heures, on ne les retrouve que dans l'épithélium des muqueuses stomacales, intestinales et de la cavité buccale ;
- après injection intrapéritonéale (i.p.), dans tous les organes ; la clairance est rapide, sauf dans le foie (24 heures) et la vessie (48 heures) où les molécules radiomarquées sont retenues dans l'épithélium des muqueuses ;
- au site d'application cutanée (45,6 mg/kg), avec de faibles quantités dans les reins et la vessie. La pénétration dans le derme et le tissu sous-cutané ne se fait qu'entre 8 et 16 heures après exposition et après une modification toxique de la peau (œdème principalement), puis les molécules radiomarquées se distribuent dans le reste de l'organisme.
Métabolisme
L'acrylate de méthyle est métabolisé par deux voies (cf. fig. 1) :
- une hydrolyse par l'intermédiaire d'une carboxylestérase (voie prépondérante) qui oxyde la molécule jusqu'à la formation de CO2 par l'intermédiaire du cycle des acides tricarboxyliques ;
- une conjugaison au glutathion qui forme deux métabolites thioéthers excrétés dans l'urine.
Schéma métabolique
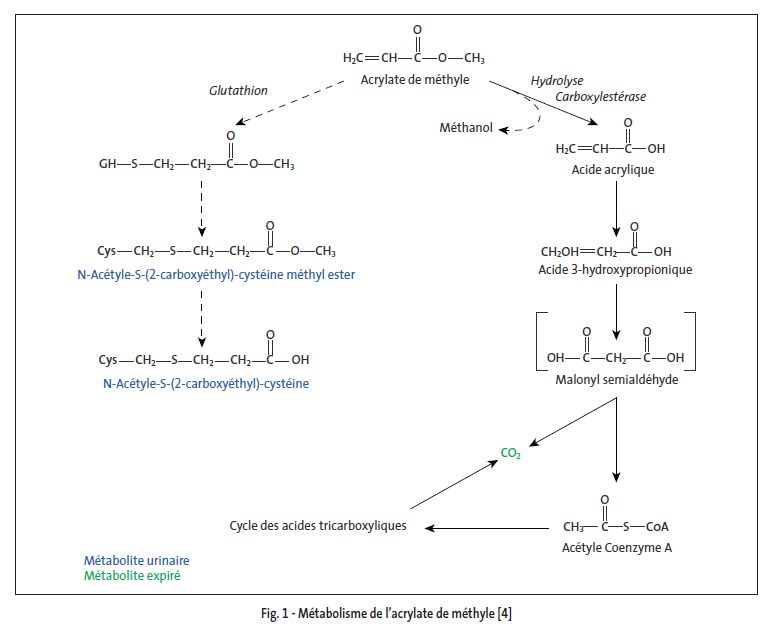
Excrétion
L'acrylate de méthyle est éliminé dans l'air expiré sous forme de CO2 (59 %) et dans l'urine (10-50 %) sous forme de deux métabolites (cf. fig. 1).
La N-acétyl-S-(2-carboxyéthyl)-cystéine urinaire représente, chez le rat, 6,6 % de la dose administrée i.p. (0,14 mmoles/kg soit 12 mg/kg) ; le dérivé ester méthylique est également décelé dans l'urine à un taux 20 fois inférieur. En cas d'injection d'un inhibiteur de la carboxylestérase (TOTP, tri-orthotolyl phosphate) avant exposition à l'acrylate de méthyle, l'excrétion de thioéthers augmente de 2 à 24 fois, avec une baisse concomitante d'excrétion de CO2.
Chez le cobaye, une exposition orale produit une excrétion urinaire de thioéthers de 13,8 % en 72 heures (11 % en 24 heures, 2,5 % le jour suivant et 0,3 % le 3e jour). L'exposition i.p. engendre 29,4 % de thioéthers (16,5 % au jour 1, 10,5 % au jour 2 et 3 % au jour 3) et 35,4 % de CO2 à 72 heures, dont plus de la moitié en 24 heures. Après exposition cutanée, l'élimination de thioéthers est beaucoup plus faible (1,2 % en 24 heures, 2 % le jour suivant et 1 % le 3e jour).
Une exposition par inhalation du rat (135 - 370 - 490 - 720 ppm soit 483 - 1320 - 1750 - 2580 mg/m3) pendant 4 heures provoque une baisse en relation avec la concentration des groupements sulfhydryles non protéiques dans les poumons, le foie et le sang ; cette baisse est accentuée par l'administration de TOTP, elle est liée au taux de baisse de la fréquence respiratoire. L'excrétion urinaire de thioéthers représente 2 à 3 % de la concentration inhalée après 6 heures d'exposition.
-
Toxicité expérimentale
-
Toxicité sur l’Homme
