Pathologie - Toxicologie
-
Toxicocinétique - Métabolisme [7]
L'acrylonitrile est largement absorbé et distribué par toutes les voies d'administration ; il est métabolisé par conjugaison directe avec le glutathion ou par oxydation par l'intermédiaire du cytochrome P450 et excrété dans l'urine sous forme d'un grand nombre de métabolites dont les ions thiocyanate et cyanure et la N-acétyl-S-(2- cyanoéthyl)cystéine ( ou acide 2-cyanoéthyl-mercapturique, CMA).
Chez l'animal
Absorption
Chez le rat, l'absorption de l'acrylonitrile est importante par voie orale (95-98 %) et par inhalation (91,5 %). Par voie orale, elle est monophasique avec un pic sanguin atteint après 3 h et une demi-vie dans le sang de 61 min. Par inhalation, l'absorption est biphasique : une phase rapide indépendante de la concentration qui dure environ 60 min. et une phase plus lente, fonction de la concentration, jusqu'à la fin de l'exposition. La baisse du taux de glutathion provoque une augmentation du taux d'absorption de l'acrylonitrile par inhalation dans les 2 phases.
Distribution
Chez l'animal, l'acrylonitrile et/ou ses métabolites s'accumulent dans le sang, le foie, les reins, la muqueuse stomacale et intestinale, les poumons et le cortex surrénalien ; la fixation aux protéines est importante. Le cœur, le thymus, la rate, les surrénales, le cerveau et la peau présentent un pic de concentration entre 3 et 6 h après l'exposition. Après 72 h, la plus forte concentration est dans le tractus gastrointestinal suggérant soit une sécrétion dans l'estomac soit une libération de l'acrylonitrile ou de ses métabolites fixés sur la muqueuse stomacale.
L'abaissement du taux de glutathion provoque une augmentation de l'acrylonitrile fixé de façon covalente dans différents organes.
Métabolisme
L'acrylonitrile est transformé par 2 voies principales (cf. fig.1) :
- conjugaison directe avec le glutathion ; du fait de la grande réactivité de l'acrylonitrile avec les centres nucléophiles, elle peut se faire avec ou sans glutathion transférase. Cette voie est considérée comme une détoxication.
- oxydation par le système de monooxygénases à cytochrome P450 avec formation d'oxyde de cyanoéthylène (CEO) ; cette voie est considérée comme une activation.
La voie prédominante est fonction de la dose systémique. La déplétion en glutathion provoque une bascule du métabolisme de la voie (1) vers la voie (2).
Le métabolite majeur dans de nombreuses espèces animales est le CMA. Les métabolites formés par conjugaison avec le glutathion représentent 85 % des métabolites urinaires.
Schéma métabolique
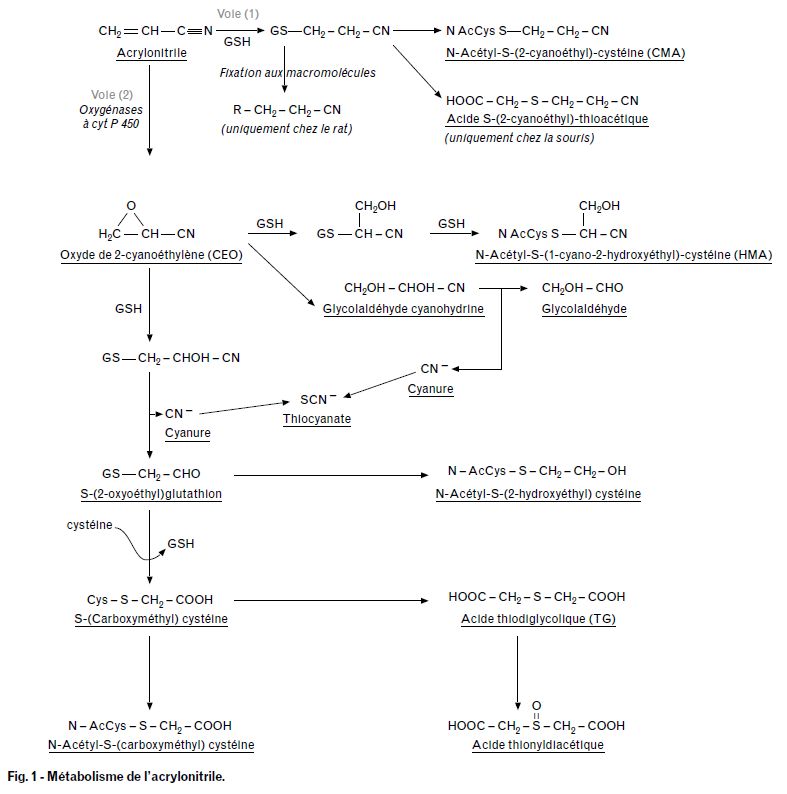
Excrétion
Le rat, après une dose orale d'acrylonitrile radiomarquée, excrète, en 24 h, 40 % des molécules marquées dans l'urine, 2 % dans les fèces, 14,3 % dans l'air expiré (4,8 % sous forme inchangée, 9 % sous forme de CO2 et 0,5 % sous forme HCN) ; 27 % des molécules marquées sont présentes dans la bile. L'excrétion totale est de 75 % de la dose initiale après 10 jours. Les cinq métabolites majeurs représentent 75-100 % des métabolites urinaires :
- la N-acétyl-S-(2-cyanoéthyl)cystéine (CMA) et l'acide S-(2-cyanoéthyl)-thioacétique issus de la voie métabolique (1) ; ils augmentent de façon non linéaire avec la dose, ce qui suggère une saturation métabolique. Cette voie est prédominante en cas d'exposition à une dose forte à court terme (par gavage ou administration iv ou ip)
- les ions thiocyanates, la N-acétyl-S-(1- cyano-2-hydroxyéthyl)cystéine (acide 2- hydroxyéthylmercapturique, HMA) et l'acide thioglycolique issus de la voie (2) prédominent lors d'exposition à de faibles doses par voie orale (dans la nourriture ou l'eau de boisson) ou par inhalation.
Durant les 9 premiers jours après une exposition par inhalation (5 ou 100 ppm soit 11 ou 220 mg/m3, pendant 6 heures, nez seul), le rat excrète respectivement 82,2 % ou 68,5 % de la dose dans l'urine, 3 ou 4 % dans les fèces et 6 ou 2,6 % dans l'air expiré sous forme de CO2. Le métabolite urinaire majeur est l'ion thiocyanate (15 -16 % de la concentration inhalée) ; le CMA ne représente que 8 % des métabolites urinaires totaux. Quand la concentration augmente l'excrétion urinaire de thiocyanate augmente, indiquant une saturation du métabolisme oxydatif.
Effets de l’espèce
La proportion de conjugués au glutathion en position 2 ou 3 détermine la quantité d'ions cyanures libérée ; les différences dans cette voie seraient responsables des différences interespèces de la toxicité induite par l'acrylonitrile.
In vitro, les microsomes de foie de souris transforment l'acrylonitrile en CEO 4 fois plus vite que ceux du rat qui sont eux-mêmes 1,5 fois plus rapides que les microsomes humains ; ceci se traduit, in vivo, par une formation plus importante de cyanures et une excrétion urinaire de thiocyanates et d'acide thiodiglycolique plus élevée chez la souris que chez le rat et l'homme.
Production d'adduits : L'acrylonitrile se fixe sur l'hémoglobine in vitro et in vivo en formant des adduits cyanoéthyl, majoritairement par réaction directe avec la cystéine. D'autres adduits peuvent aussi être formés par réaction avec la valine N-terminale (CEVal) ; ils semblent être plus spécifiques de l'acrylonitrile. La quantité d'adduits formés n'est pas linéaire avec la dose d'exposition, elle est le reflet de la quantité d'acrylonitrile circulant dans le sang et augmente avec la consommation de tabac.
Surveillance Biologique de l'exposition
Etant donné le risque de passage percutané de l’acrylonitrile, la surveillance biologique de l’exposition professionnelle (SBEP) est intéressante.
Le dosage de l'acrylonitrile dans les urines en fin de poste de travail a été proposé pour la SBEP. Ce paramètre est plus ou moins bien corrélé aux concentrations atmosphériques. Des taux non nuls sont retrouvés chez les sujets non professionnellement exposés (rôle du tabac).
Le dosage urinaire des thiocyanates en fin de poste de travail a été proposé pour la SBEP. Mais ce paramètre n'est pas spécifique (influence du tabac, de l'alimentation) et à de faibles niveaux d'exposition (1 ppm), il ne permet pas de différencier exposés et non exposés. Des taux non nuls sont retrouvés chez les sujets non professionnellement exposés (rôle du tabac).
Le dosage des adduits à l'hémoglobine (adduits N-cyanoéthylvaline) est un paramètre spécifique qui reflète l'exposition des 3 mois précédents. IL peut être utile, lors d'une exposition aiguë, pour apprécier l'imprégnation à distance de l'accident (jusqu'à 3 mois). La Commission allemande, lors d'une exposition à l'acrylonitrile recommande le dosage de N-2-cyano-éthylvaline dans les érythrocytes avec un taux de 420 µg/L, pour une exposition à 7 mg/m3 (3 ppm) (valeur EKA). Des taux non nuls sont retrouvés chez les sujets non professionnellement exposés.
Le dosage de l'acide cyanoéthylmercapturique dans les urines en fin de poste a également été proposé pour la SBEP. Etant donné la très grande variabilité interindividuelle de ce paramètre, son utilisation au niveau individuel n’est pas conseillée.
Il n’existe pas de valeur biologique d’interprétation pour la population professionnellement exposée.
-
Toxicité expérimentale
-
Toxicité sur l’Homme [7, 14, 15, 17]
