Toxicité aiguë [1 à 4]
Le diphényle est modérément toxique par voie orale, inhalatoire ou cutanée. Il n'endommage que très légèrement la muqueuse oculaire.
La DL50 orale est égale à 3280 mg/kg chez le rat, 2410 mg/kg chez la souris et 2400 mg/kg chez le lapin. Par inhalation, la CL50 est supérieure à 200 mg/m3 chez le rat. Par voie cutanée, chez le lapin, la DL50 est égale à 2500 mg/kg pendant 24 heures.
Les symptômes d’une intoxication orale, chez le rat, sont une augmentation de la fréquence respiratoire, une décharge lacrymale, une anorexie associée à une perte de poids, une faiblesse musculaire, une ataxie ; la mort survient par coma 2 heures à 18 jours après l’exposition.
L’examen anatomo-pathologique révèle, chez le rat et le lapin, une congestion viscérale et des lésions du foie (dégénérescence cellulaire), des reins (modifications nécrotiques associées à une néphrite glomérulo-tubaire), du cœur (modifications dégénératives du myocarde) et des poumons (congestion et œdème alvéolaire). Le poumon, le foie et les reins sont également la cible du diphényle administré par voie cutanée.
Le diphényle n’est pas irritant pour la peau du lapin (0,5 mg/kg/j à 25 % dans l’huile d’olive, 5 j/sem jusqu’à 20 applications) ; déposé dans l’œil du lapin (100 mg), il provoque une irritation légère, réversible en 7 jours, accompagnée d’une abondante décharge lacrymale.
Toxicité subchronique, chronique [1 à 3, 5, 6]
La toxicité chronique du diphényle varie avec la voie d’exposition et l’espèce, la plus sensible étant la souris. La cible principale est le système urinaire, un effet moindre est observé sur le foie et les paramètres sanguins.
Des expositions orales répétées à forte dose (> 0,5 % dans la nourriture, 2 ou 13 mois), agissent sur la croissance et la longévité des animaux et affectent les reins (augmentation de poids, dilatation du tube rénal, modifications polykystiques, augmentation du volume et de la densité urinaires), le foie (modifications dégénératives associées à une altération des fonctions thyroïdienne et parathyroïdienne), le sang (baisse du taux d’hémoglobine) et la rate.
Les modifications induites sur le système urinaire sont variables selon l’espèce et la voie.
Par voie orale :
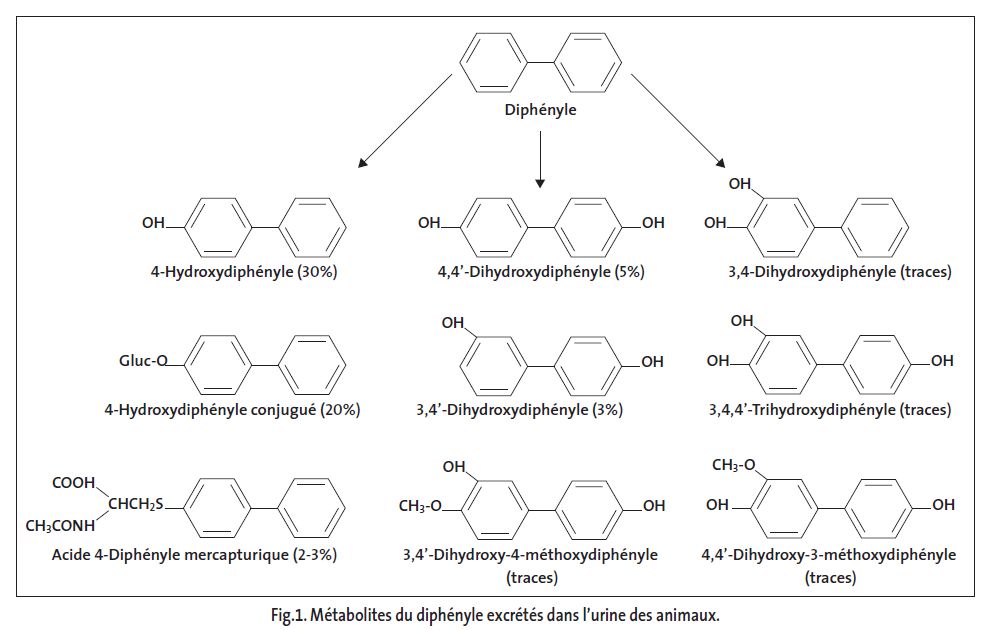
- les rats exposés à 5 000 mg/kg dans la nourriture pendant 24 semaines (≈ 375 mg/kg/j) forment des microcalculs, présents, après 16 semaines, dans l’urine, l’uretère, la vessie et les reins et développent une hyperplasie de la vessie (simple ou diffuse). Au niveau rénal, on observe pyélonéphrite, atrophie tubaire et fibrose. Le sédiment urinaire est formé de 4-hydroxydiphényle et de son conjugué avec l’acide glucuronique. Les effets urinaires sont complètement réversibles, les effets rénaux partiellement. La NOAEL est de 1000 mg/kg dans la nourriture pendant 24 semaines.
- la souris, au contraire, après administration de 10 000 mg/kg dans la nourriture pendant 32 semaines (1500 mg/kg/j), présente une baisse de la concentration urinaire en sodium et une néphrite interstitielle rénale, mais pas d’hyperplasie de la vessie [7].
Par inhalation (poussière de diphényle imprégnée sur de la zéolite, 5, 40 ou 300 mg/m3, 7 h/j, 5j/sem, 13 sem) :
- les lapins sont insensibles ;
- les rats montrent, à 40 mg/m3, une irritation de la muqueuse nasale et à 300 mg/m3 une respiration difficile avec lésions broncho-pulmonaires, un léger effet toxique sur le foie et les reins et une augmentation de la létalité ;
- les souris sont les plus sensibles : à 5 mg/m3, il y a augmentation de la létalité, irritation du tractus respiratoire supérieur et inflammation broncho-pulmonaire.
Effets génotoxiques [1, 3, 8, 9, 10]
Au vu de la diversité des réponses obtenues aux tests pratiqués, il n’est pas possible de définir le pouvoir mutagène du diphényle.
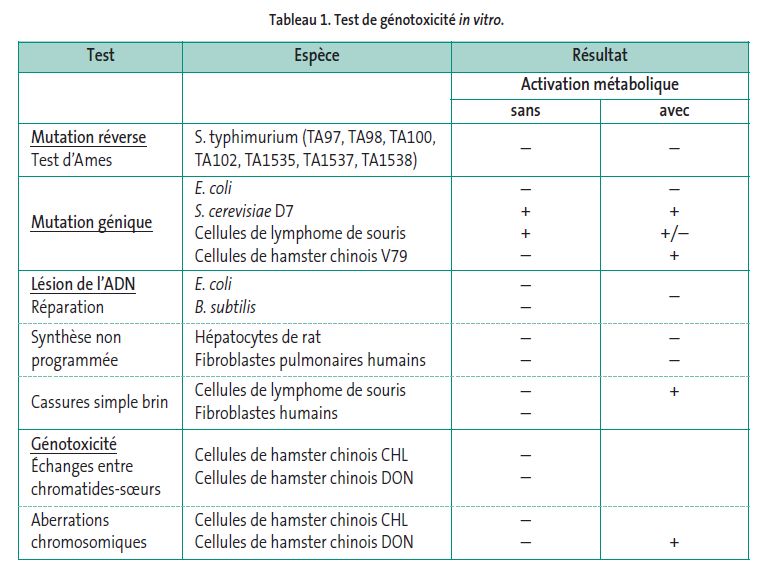
In vitro, les résultats des tests effectués avec le diphényle sont très variables (tableau 1).
In vivo, une étude insuffisamment documentée n'a pas permis de constater la présence d'aberrations chromosomiques dans la moelle osseuse de rats exposés au diphényle par voie respiratoire (10 ou 50 ppm, 7 h/j, 5 j/sem, 30 jours)[11]. Le test des comètes (mesure de lésions de l’ADN), effectué chez la souris, exposée à 2000 mg/kg par voie orale, est positif dans tous les organes mesurés (estomac, foie, rein, vessie, poumon, cerveau, moelle osseuse), avec un maximum à 24 heures [12].
Effets cancérogènes [1, 6, 13]
Le diphényle n’est pas cancérogène pour le rat ou la souris ; en revanche, il est promoteur de l’effet cancérogène induit par d’autres substances chimiques.
Il n’y a pas d’augmentation du taux de tumeurs après exposition de rats, par voie orale, à 94 mg/kg/j pendant 104 semaines ; à 375 mg/kg/j pendant 75 semaines, on observe une hyperplasie et une papillomatose de l’épithélium de la vessie et, à 338 mg/kg/j pendant 104 semaines, chez les mâles uniquement, des lésions néoplasiques de la vessie (papillomes et carcinomes), avec hyperplasie et métaplasie de l’épithélium et présence de calculs. Chez la souris, une administration de 300 ou 900 mg/kg/j pendant 104 semaines, dans la nourriture, provoque l’apparition d’adénomes et de carcinomes hépatiques chez les femelles, mais sans relation dose-effet.
Le diphényle est promoteur de la cancérogenèse induite par la N-butyl-N’-hydroxybutylnitrosamine (BBN) chez le rat (0,05 % de BBN dans l’eau de boisson pendant 4 semaines puis 0,5 % de diphényle dans la nourriture pendant 32 semaines) ; ces animaux développent une hyperplasie (94 %), des papillomes (83 %) et des carcinomes (61 %) de la vessie, contrairement aux animaux exposés uniquement au BBN ou au diphényle qui ne présentent pas de tumeur. Des souris, prétraitées par le BBN et recevant une nourriture contenant 1500 mg/kg/j de diphényle pendant 32 semaines, ne développent pas de tumeur [7].
Effets sur la reproduction [1, 3, 14]
Des informations limitées semblent indiquer que le diphényle n’est pas foetotoxique ou tératogène même à des doses toxiques pour les mères.
Administré par gavage, du 6e au 15e jour de gestation, chez le rat, le diphényle est létal pour les mères et légèrement fœtotoxique (non statistiquement significatif) à des concentrations supérieures à 500 mg/kg/j. Il n’induit pas d’effet s’il est administré dans la nourriture (0,5 %) pendant 1 génération, du 60e jour avant l’accouplement jusqu’au sevrage ; si la dose est de 1 % pendant 3 générations, il diminue légèrement la fertilité des femelles, la taille de la portée et le taux de croissance des jeunes rats, sans augmentation de l’effet lors des générations successives.