Prélèvement : Actif sur cassette avec filtres imprégnés
Analyse : chromatographie ionique avec suppression détection conductimétrique
Données de validation : Validation complète
Substances
Informations générales
Propriétés physico-chimiques
| Nom | N° CAS | Formule chimique | Classification CMR |
|---|---|---|---|
| Acide acétique | 64-19-7 | C2H4O2 |
|
Plus d'informations
| Nom | Masse molaire | Densité | Synonymes | Fiche toxicologique |
|---|---|---|---|---|
| Acide acétique | 60,06 | 1,049 | Acide éthanoïque |
Familles de substances
- ACIDES CARBOXYLIQUES ALIPHATIQUES
Principe et informations
Cette méthode a été validée en suivant les référentiels normatifs. Toutes les données de validation ainsi que les calculs des performances de la méthode sont indiqués dans les données de validation.
Principe de prélèvement et d'analyse
-
État physique
Aérosols (mélange de gaz ou vapeurs / particules) -
Type de prélèvements
Actif -
Nom du dispositif
cassette avec filtres imprégnés -
Plus d'informations
-
Technique analytique
CHROMATOGRAPHIE IONIQUE AVEC MEMBRANE DE SUPPRESSION -
Injecteur
PASSEUR AUTOMATIQUE -
Détecteur
CONDUCTIMETRIE
Domaine d'application
| Substance | Quantité minimum sur le dispositif | Quantité maximum sur le dispositif | Concentration minimum | Concentration maximum | Volume maximum |
|---|---|---|---|---|---|
| Acide acétique | 4 µg |
240 µg |
0,9 mg/m3 |
53 mg/m3 |
4,5 L |
Réactifs
- ACIDE ACETIQUE
- ACIDE SULFURIQUE
- CARBONATE DE SODIUM
- EAU
- HYDROXYDE DE POTASSIUM
- SOLUTION ETALON 1g/L
Méthode de prélèvement
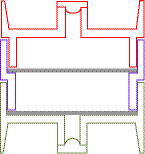
Utilisation de la cassette fermée pour le prélèvement d’aérosols
Un dispositif de prélèvement :
Dispositif N°1
-
Type dispositif
CASSETTE 37 mm 3 pièces -
Support ou substrat de collecte
- 2 FILTRES EN FIBRE DE QUARTZ IMPREGNES
-
Préparation du substrat
La solution d’imprégnation est obtenue par dissolution de 5 g de Na2CO3 dans de l’eau et jaugeage à 100 mL. Soumettre éventuellement aux ultrasons (ou agitation magnétique) pour favoriser la solubilisation.
Les filtres en fibre de quartz sont imprégnés de 600 µL de solution d'imprégnation. Faire sécher à l’étuve à 60°C pendant 2 h ou sous sorbonne pendant 24 h dans un local exempt de toute pollution.
-
Commentaires, conseils et consignes
Un filtre est déposé au fond de la cassette et le second sur la pièce intermédiaire. Durant ces opérations, les filtres seront manipulés avec une pince.
Conditions de prélèvement
-
Débit de prélèvement mini (L/min)
0,250 -
Débit de prélèvement maxi (L/min)
0,300 -
15 minutes (VLEP-CT possible dans ces conditions)
oui
Pompe de prélèvement
- Pompe à débit de 0,02 à 0,5 L/min
Compléments
Utiliser des filtres traités haute température (SKC ou équivalent) pour obtenir la limite de quantification la plus basse (voir Sélection du support de collect dans les données de validation).
Analyser des blancs de laboratoire pour déterminer la quantité d'acide déjà présente sur le support et l'homogénéité des lots avant leur utilisation.
Préparation des dispositifs de prélèvement en vue d’une intervention en entreprise
Méthode d'analyse
Principe général de l'analyse en laboratoire
Préparation d'analyse
-
Durée de conservation prélèvements avant analyse
1 mois -
Conditions de conservation avant analyse
Avant le prélèvement, les filtres imprégnés peuvent être conservés 6 mois, dans un local exempt de toute pollution.
Remarque : des blancs de laboratoire devront être réalisés avant utilisation des filtres pour s’assurer qu’il n’y a pas de pollution.
Si l'acide acétique n'est pas extrait très rapidement du support, il y aura migration d’une partie de l’acide acétique prélevé d’un support imprégné sur l’autre (Voir données de validation).
-
Séparation des plages
oui -
Nombre d'étapes de préparation
1 -
Conditions de conservation échantillon préparé avant analyse
Une étape de préparation :
Étape de préparation N°1
-
Séparation des plages
oui -
Solvant ou solution
- EAU
- ELUANT
-
Type de préparation
Désorption -
Volume
20 mL -
Ultrasons
- Temps d'ultrasons : 5 min
-
Autres conditions de préparation
- Ouvrir la cassette et transférer chaque filtre imprégné dans un flacon de désorption.
- Ajouter 10 à 20 mL d’eau ou d’éluant.
- Agiter aux ultrasons environ 5 minutes.
- Filtrer sur cartouche Millex (0,22 µm) ou sur membrane (0,45 µm) et analyser.
-
Commentaires
Remarque :
- Traiter les blancs de laboratoire et les blancs de terrain de la même façon.
Une condition analytique :
Condition analytique N°1
-
Technique analytique
- CHROMATOGRAPHIE IONIQUE AVEC MEMBRANE DE SUPPRESSION
-
Injecteur
- PASSEUR AUTOMATIQUE
-
Colonne
- ECHANGEUSE D'IONS
- SUPRESSEUR
-
Détecteur
- CONDUCTIMETRIE
Étalonnage et expression des résultats
La méthode d'étalonnage indiquée est celle utilisée lors du développement. Elle n'a cependant pas de caractère obligatoire
-
Principe d'étalonnage
externe -
Solvant de l’étalon
- Même solvant que celui des échantillons
-
Commentaires
Réaliser des étalons à partir de substances de référence, commerciales ou synthétisées en laboratoire. Le solvant utilisé pour réaliser les solutions sera celui choisi pour le traitement des échantillons.
Préparer une gamme d'étalonnage, dans la même matrice que les échantillons (ne pas oublier le filtre imprégné)
-
Calcul de la quantité de substance sur le dispositif
La concentration réelle C (en mg/m3) dans l’air est donnée par :
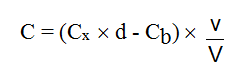
avec :
Cx (mg/L) : concentration de la substance dans l'échantillon
d : facteur de dilution
Cb ( mg/L) : concentration moyenne de la substance dans les blancs de laboratoire
v (mL) : volume de jaugeage
V (L) : volume d’air prélevé
Compléments
Diluer si nécessaire les échantillons avec du blanc filtre (filtres désorbés dans de l’eau ou de l’éluant dans les mêmes conditions que les échantillons) de façon à rester dans la gamme d'étalonnage.
Des exemples de conditions d'analyse sont détaillés dans les données de validation.
Interférences
Les chlorures d’acides sont hydrolysés en acides carboxyliques et acides hydrochloriques sur les supports solides, dans l’air humide, et en solution. Par conséquent, en présence de chlorure(s) d’acide(s), la méthode d’échantillonnage peut surestimer la concentration en acide carboxylique dans l’air.
Les fluorures et les formates peuvent également interférer sur les dosages nécessitant une adaptation des conditions d’analyse.
Remarque :
Les analyses peuvent être réalisées en électrophorèse capillaire après validation de la méthode.
Bibliographie
- NF EN 482 – Exposition sur les lieux de travail. Exigences générales concernant les performances des procédures de mesure des agents chimiques. La Plaine Saint Denis, Association française de normalisation (AFNOR), 2012, 18 p.
- NF EN 13890 – Exposition sur les lieux de travail. Procédures pour le mesurage des métaux et métalloïdes dans les particules en suspension dans l'air - Exigences et méthodes d'essai. La Plaine Saint Denis, Association française de normalisation (AFNOR), 2009, 36 p.
- NF EN 1076 – Exposition sur les lieux de travail. Procédures pour le mesurage des gaz et vapeurs à l’aide de dispositifs de prélèvement par pompage. La Plaine Saint Denis, Association française de normalisation (AFNOR), 2010, 36 p.
- V. OURY, A. PELTIER - Prélèvement et dosage de l'acide acétique par chromatographie ionique. Cahiers de notes documentaires - Hygiène et sécurité du travail, n° 187, 2e trimestre 2002, pp. 89-99.
- ANSES – Rapport d’expertise collective du CES « Expertise en vue de la fixation de valeurs limites à des agents chimique en milieu professionnel » : Paris, Agence nationale de sécurité sanitaire de l’alimentation, de l’environnement et du travail (ANSES), 2012, 47 pages.
- V. OURY, A. PELTIER - Prélèvement et dosage de l'acide formique par chromatographie ionique. Cahiers de notes documentaires - Hygiène et sécurité du travail, n° 195, 2e trimestre 2004, pp. 53-61.
Historique
| Version | Date | Modification(s) faisant l’objet de la nouvelle version | Paragraphes concernés |
|---|---|---|---|
| 78 | 11/09/2003 | Création et mises à jour | |
| 078/V02.01 | 01/10/2015 | Nouvelle présentation | Tous |
| Ajout des annexes avec données de validation de l’acide acétique | Annexes 2 et 3 | ||
| Anciennes données de validation recalculées | Annexe 4 | ||
| M-321/V01 | Janvier 2016 | Mise en ligne Substance unique Prélèvement sur cassette avec filtres imprégnés Analyse par chromatographie ionique avec suppression. |
Date de mise à jour : janvier 2016
Ancien numéro de fiche MétroPol : 078
