Prélèvement : Actif sur cassette et membrane en ester de cellulose
Analyse : spectrométrie d'émission à plasma
Données de validation : Validation partielle
Substances
Informations générales
Propriétés physico-chimiques
| Nom | N° CAS | Formule chimique | Classification CMR |
|---|---|---|---|
| Métaux - Métalloïdes |
Plus d'informations
| Nom | Masse molaire | Densité | Synonymes | Fiche toxicologique |
|---|---|---|---|---|
| Métaux - Métalloïdes |
Familles de substances
- METALLOIDES
- METAUX
Principe et informations
Cette méthode concerne le prélèvement et l’analyse d’aérosols contenant des métaux et métalloïdes, prélevés au moyen d'une cassette fermée (orifice 4 mm) munie d'une membrane en ester de cellulose (MEC).
Pour le prélèvement de la fraction inhalable, l'aérosol prélevé ne doit pas avoir une granulomètrie trop élevée (diamètre aérodynamique inférieur à 20 µm environ).
Les particules captées (retenues dans la cassette, que ce soit sur la membrane ou sur les parois) sont mises en solution à même la cassette ayant servi au prélèvement par des acides appropriés.
Cette méthode s'applique à la mesure de la concentration des éléments totaux dans l'air, qu'ils soient seuls ou sous forme combinée. Les aspects liés à la spéciation ne sont pas pris en compte dans cette méthode.
Remarques :
- Après mise en solution par l'une des méthodes décrites dans cette fiche, l'analyse par spectrométrie de masse avec plasma à couplage inductif (ICP-MS) peut être utilisée également en fonction de la sensibilité requise ou du matériel disponible dans le laboratoire.
- L'utilisation de la spectrométrie d'absorption atomique (flamme ou atomisation électrothermique) est possible également, si elle présente une sensibilité suffisante pour l’élément analysé (voir les fiches métaux et métalloïdes correspondantes).
Précautions particulières
- L'acide perchlorique est susceptible de provoquer des explosions s'il est mis en présence de quantités importantes de matières organiques et surtout lorsqu'il est chauffé. Ce risque n'existe pas dans la plupart des cas relatifs à la détermination des métaux dans l'air des lieux de travail, surtout si les solutions ne sont pas chauffées. En cas de présence de quantités importantes de matières organiques, utiliser une autre méthode de minéralisation des membranes en ester de cellulose que celle décrite dans la présente fiche.
- Certaines des opérations décrites ci-après entraînent la manipulation d’acide fluorhydrique qui présente un danger spécifique important. Il est impératif de manipuler toutes les solutions fluorhydriques avec des gants et des lunettes de protection ; toutes les manipulations doivent être effectuées sous sorbonne. S’assurer de la présence à proximité de l’opérateur de gel au gluconate de calcium. En cas de contact accidentel, effectuer un rinçage abondant à l’eau et traiter immédiatement la peau avec du gel au gluconate de calcium avant l’apparition de la douleur.
- Si la méthode retenue implique l'utilisation d'acide fluorhydrique, il est recommandé d’ajouter du carbonate de calcium dans le flacon de récupération de l'appareil pour neutraliser les solutions évacuées.
- Attention au bouchage éventuel du drain par le fluorure de calcium (CaF2) formé, qui est insoluble.
- Tout le matériel utilisé dans les différentes manipulations de l’acide fluorhydrique doit être en plastique et si possible à usage unique. En effet, cet acide attaque le verre. Vérifier également l’absence d’impureté susceptible d’être diffusée par les flacons en plastique (surtout si les flacons sont teintés). En cas d'utilisation de flacons de faible diamètre (pour passeur d'échantillons par exemple), les placer toujours dans un portoir adapté pour éviter les risques de renversement.
Principe de prélèvement et d'analyse
-
État physique
Particules en suspension (liquides ou/et solides) -
Type de prélèvements
Actif -
Nom du dispositif
cassette et membrane en ester de cellulose -
Plus d'informations
-
Technique analytique
SPECTROMETRIE D'EMISSION A PLASMA (ICP/AES)
Réactifs
- ACIDE CHLORHYDRIQUE
- ACIDE FLUORHYDRIQUE
- ACIDE NITRIQUE
- ACIDE PERCHLORIQUE
- CARBONATE DE CALCIUM
- EAU
- GEL DE GLUCONATE DE CALCIUM
- SOLUTION ETALON 1g/L
Méthode de prélèvement
Utilisation de la cassette fermée pour le prélèvement d’aérosols
Un dispositif de prélèvement :
Dispositif N°1
-
Type dispositif
CASSETTE POLYPROPYLENE 37 mm 3 pièces -
Support ou substrat de collecte
- MEMBRANE EN ESTERS DE CELLULOSE
- TAMPON EN CELLULOSE
-
Préparation du substrat
Membrane en esters de cellulose mixte porosité 0,8 µm.
-
Commentaires, conseils et consignes
Un tampon de cellulose est déposé au fond de la cassette et la membrane juste au dessus.
Conditions de prélèvement
-
Débit de prélèvement (L/min)
2 -
15 minutes (VLEP-CT possible dans ces conditions)
oui -
Temps de prélèvement maximum en heures
8
Pompe de prélèvement
- Pompe à débit de 1 à 3 L/min
Compléments
Voir données de validation - compléments : Eléments de choix du filtre de prélèvement.
Un dispositif analogue peut être utilisé pour le prélèvement de la fraction alvéolaire d'un aérosol en faisant précéder la cassette d'un cyclone nylon 10 mm (Voir Utilisation du cyclone pour le prélèvement d’aérosols ).
Préparation des dispositifs de prélèvement en vue d’une intervention en entreprise
Méthode d'analyse
Principe général de l'analyse en laboratoire
Préparation d'analyse
-
Conditions de conservation avant analyse
Les éléments prélevés sont stables indéfiniment.
-
Nombre d'étapes de préparation
1 -
Commentaires sur les étapes
La mise en solution est réalisée en 2 étapes :
- Mise en solution de la membrane à froid par HClO4 puis
- Mise en solution de l’aérosol par un mélange d’acides approprié, HCl+ HNO3 par exemple, (avec ou sans HF en fonction de l'aérosol étudié) pour la recherche des éléments totaux.
Deux modes opératoires décrits ci-dessous peuvent être utilisés : mode opératoire avec jaugeage et sans jaugeage de la solution.
Une étape de préparation :
Étape de préparation N°1
-
Type de préparation
Solubilisation -
Ultrasons
- Temps d'ultrasons : 10 min
-
Autres conditions de préparation
Préambule : Dans le cas d’une solubilisation incomplète, il sera nécessaire de mettre en œuvre un protocole différent de celui décrit ci-dessous.
Deux modes opératoires sont utilisables : avec jaugeage ou sans jaugeage de la solution. On choisira celui qui présente les meilleurs avantages pour le dosage à effectuer par la suite.
Ces modes opératoires prennent en compte les dépôts éventuels d'éléments métalliques sur les parois de la cassette porte-filtre.
Dans les deux cas, commencer par nettoyer l’extérieur de la cassette (avec une lingette humide par exemple) pour éviter toute pollution éventuelle lors de l’ouverture de celle-ci. Ensuite, ôter le tampon de cellulose ayant servi de support à la membrane pendant le prélèvement en ayant soin de retourner la cassette avant de l’ouvrir (orifice d’entrée vers le bas). Pendant cette opération, veiller à laisser la membrane en place, au contact de la partie supérieure de la cassette (côté orifice d'entrée). Cette précaution a pour but d'éviter de perdre des particules éventuellement déposées sur les parois. Refermer la cassette avant toute autre manipulation.
Mode opératoire avec jaugeage de la solution
- Après avoir vérifié le serrage des différents éléments de la cassette, et la présence du bouchon inférieur, introduire 0,5 mL d’acide perchlorique concentré par l'orifice d'entrée de l'air, à l'aide d'une pipette automatique à embout jetable. Attendre environ ½ heure avant d’ajouter 2 mL d’un mélange d’acides, par exemple 2 volumes HNO3 + 1 volume HCl + 1 volume HF.
Remarque : on n'utilisera l’acide fluorhydrique que si la nature de la poussière le nécessite.
- Reboucher la cassette et l'introduire dans une cuve à ultrasons contenant de l'eau ultrapure.
- Soumettre à l'agitation ultrasonique pendant 10 minutes, en retournant la cassette après 5 minutes. On peut, si nécessaire, chauffer l'eau de la cuve, jusqu'à 60°C, après avoir pris la précaution d'enlever le bouchon supérieur de la cassette.
- Rincer l'extérieur de la cassette avec de l'eau ultrapure, puis essuyer l'extérieur ou égoutter avant de transvaser dans un tube gradué.
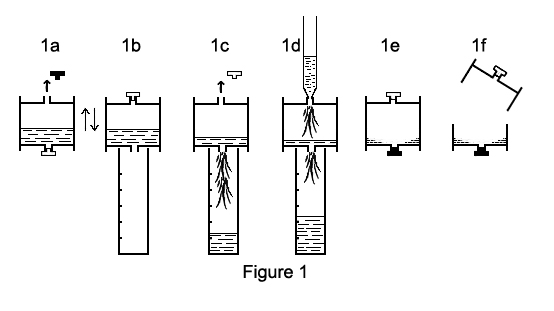
- Les phases de transvasement et de rinçage sont effectuées selon la séquence décrite dans la figure 1 :
- enlever le bouchon de l'orifice de sortie (fig. 1a),
- retourner la cassette sur un tube gradué (fig. 1b),
- enlever le bouchon restant (fig. 1c), ce qui a pour effet de vider le contenu de la cassette dans le tube.
- rincer avec deux fois 5 mL d'eau ultrapure, l'introduction se faisant à l'aide d'une pipette automatique par l'orifice supérieur (fig. 1d),
- remettre les bouchons (fig. 1e),
- ouvrir la cassette (fig. 1f). Transvaser le reliquat de solution dans le tube, rincer les parois des deux parties de la cassette et amener au volume v (v = 20 mL par exemple), avec de l'eau ultrapure.
Les cassettes ayant servi à ces mises en solution ne sont pas réutilisables, elles sont jetées.
Mode opératoire sans jaugeage de la solution
- Après avoir vérifié le serrage des différents éléments de la cassette, et la présence du bouchon inférieur, introduire 0,5 mL d’acide perchlorique concentré par l'orifice d'entrée de l'air, à l'aide d'une pipette automatique à embout jetable. Attendre environ ½ heure avant d’ajouter 2 mL d’un mélange d’acides, par exemple 2 volumes HNO3 + 1 volume HCl + 1 volume HF.
Remarque : on n'utilisera l’acide fluorhydrique que si la nature de la poussière le nécessite
- Reboucher la cassette et l'introduire dans une cuve à ultrasons.
- Soumettre à l'agitation ultrasonique pendant 10 minutes, en retournant la cassette après 5 minutes.
- Introduire ensuite 10 mL d'eau ultrapure à l'aide d'une pipette automatique à embout jetable par l'orifice d'entrée de l'air. Reboucher et homogénéiser.
- Pour l'analyse, introduire directement le capillaire du spectrophotomètre par l'orifice supérieur de la cassette.
- Si l'on veut transvaser la solution (par exemple dans un tube de passeur), ôter l'un des bouchons, retourner la cassette sur le tube, puis soulever l'autre bouchon en le maintenant en place pour réguler l'écoulement.
Avantages de la méthode avec jaugeage
- Volume de solution permettant de doser plusieurs éléments avec un spectrophotomètre séquentiel (SAA ou spectrophotométrie d’émission à plasma).
- Solution finale moins concentrée en acides, donc moins dangereuse pour le manipulateur s'il vient à être en contact avec la solution et moins corrosive pour le matériel.
Avantages de la méthode sans jaugeage
- Volume de solution plus faible permettant d'atteindre des concentrations plus basses sur le filtre.
- Moins de manipulations des acides.
- Moins de risques de renversement.
- Pas d'utilisation de tubes gradués.
- Pas de risque d'erreur lors du report des identifiants de la cassette sur le tube.
-
Commentaires
- Dans le cas d'une solubilisation incomplète, il est nécessaire d'utiliser un mode opératoire différent, mettant en jeu des procédures de dissolution plus efficaces, par exemple en transvasant quantitativement la solution et les particules non dissoutes dans un réacteur de digesteur micro-ondes. Pour certains aérosols très fins (par exemple des fumées de soudage), la nébulisation de la suspension obtenue est possible et peut donner des résultats équivalents à ceux obtenus avec une solubilisation totale "slurry nebulisation". Ceci doit avoir été vérifié avant toute analyse d'une série d'échantillons non solubilisés.
- Traiter les blancs de laboratoire et balncs de terrain de la même façon.
Une condition analytique :
Condition analytique N°1
-
Technique analytique
- SPECTROMETRIE D'EMISSION A PLASMA (ICP/AES)
-
Commentaires, conseils ou condition particulières
Réglage de l’appareil et essais préliminaires
-
Pour la détermination des éléments totaux ou insolubles, s’assurer que l’appareil est bien équipé d’un matériel de travail résistant à l’acide fluorhydrique (nébuliseur, chambre de nébulisation et injecteur).
Dans la mesure où l’appareil et le volume de solution disponible le permettent, effectuer une analyse qualitative de quelques échantillons représentatifs de la série d’échantillons à analyser. En déduire les éléments à déterminer : ceux relevant de l’hygiène industrielle (toxiques ou traceurs) et ceux pouvant interférer sur l’analyse.
- Choisir pour chaque élément la (ou les) longueur(s) d’onde de mesure en fonction de la gamme de concentration attendue et des interférents possibles (provenant de l’échantillon ou du filtre). Fixer les points de correction de fond.
- Effectuer les préréglages nécessaires (alignement de la torche, profilage en longueur d’onde, etc.) et déterminer les paramètres du plasma selon les instructions du constructeur.
- Déterminer le délai avant le début d’une mesure, le nombre et le temps de lecture donnant des résultats satisfaisants (choisir le meilleur compromis pour le nombre et la durée des lectures).
- Déterminer les coefficients de correction inter-éléments si les interférences n’ont pas pu être toutes évitées (ces coefficients peuvent parfois être calculés automatiquement pendant l’étalonnage du spectromètre, il s’agit alors d’en vérifier la pertinence).
- Sauvegarder ces paramètres dans la méthode.
Interférences
- En spectrométrie d’émission à plasma, les interférences spectrales trouvées dans la littérature seront soit évitées par le choix d’une raie analytique alternative, soit corrigées après mesure (si possible simultanée) de l’interférent.
-
Étalonnage et expression des résultats
La méthode d'étalonnage indiquée est celle utilisée lors du développement. Elle n'a cependant pas de caractère obligatoire
-
Principe d'étalonnage
externe -
Solvant de l’étalon
- Même solvant que celui des échantillons
-
Commentaires
Préparation des solutions étalons
- Utiliser des filtres du même type que ceux utilisés pour le prélèvement.
- L’homogénéité des filtres par lots doit être vérifiée et une valeur de blanc filtre moyen doit être déterminée pour 6 filtres minimum. Les solutions étalons sont préparées dans une matrice reconstituée.
- Les solutions étalons sont préparées directement à partir de une ou deux solution(s) mère(s) à 1 g/L. Si on souhaite utiliser une ou des dilution(s) intermédiaire(s), préparer plusieurs solutions indépendantes, de façon à pouvoir repérer une éventuelle erreur de dilution. Les étalons sont préparés par dilution volume à volume de "double" étalon avec du "double" blanc filtre :
- double étalon : solution aqueuse de concentration double de celle souhaitée dans l’étalon final,
- double blanc filtre : x filtres sont dissous dans 0,5 x mL HClO4 (attendre environ 30 min.). Ajouter 2 x mL du même mélange acide que celui utilisé pour le mise en solution des échantillons. Jauger à (x/2 v) mL avec de l’eau (v est le volume de jaugeage utilisé lors de la mise en solution des filtres).
Remarques
Une alternative à cette méthode de préparation des étalons est la suivante :
- y mL de solution étalon concentrée (1 g/L ou 100 mg/L),
- 5 mL de blanc filtre concentré (x filtres + 0,5 x mL HClO4 + 2 x mL de mélange acide, avec par exemple x = 50),
- jaugeage à v mL avec de l’eau.
- L’étalon zéro ETA0 (ou solution de tarage - cf. NF T 01-041) est réalisé soit par dilution volume à volume du double blanc filtre avec de l’eau, soit par dilution du blanc filtre concentré (exemple : 5 mL de blanc filtre concentré - jaugeage à v mL).
- La gamme de travail retenue couvrira de préférence un domaine où la réponse de l’appareil est linéaire ou présente une faible déviation à la linéarité (voir critère de courbure dans "données de validation - compléments"). Dans ce dernier cas, le nombre minimal d’étalons sera de 5 afin de pouvoir mieux déterminer à partir de quelle valeur se situe le début de l'écart à la linéarité.
- Dans le cas de la préparation d’étalons multi-élémentaires, et en particulier pour les analyses par ICP, préparer les solutions étalon de telle façon que le rapport des concentrations des différents éléments ne soit pas constant et que la charge saline totale soit pour tous du même ordre de grandeur.
Étalonnage
- Définir la gamme d’étalonnage et étalonner l’appareil, l’auto-zéro étant fait sur ETA0.
- Tracer la courbe d’étalonnage.
Dosage
En règle générale, on passe 5 à 10 échantillons (filtres prélevés et vierges), puis on passe l’étalon de contrôle ETAQC et l’étalon ETA0 pour vérifier la stabilité de l’appareil. Passer également des échantillons dilués par 2 ou 4 dans ETA0 pour chaque type de poussière afin de vérifier un éventuel effet de matrice.
Pour les analyses, il est recommandé de suivre le protocole décrit dans "données de validation - compléments".
Bibliographie
- NF ISO 15202-2 (X 43-265-2) - Décembre 2001. Air des lieux de travail. Détermination des métaux et métalloïdes dans les particules en suspension dans l'air par spectrométrie d'émission atomique avec plasma à couplage inductif - Partie 2 : Préparation des échantillons. Paris-La-Défense, AFNOR, 2001, 49 p.
- NF ISO 15202-2 (X 43-265-3) - Décembre 2005. Air des lieux de travail. Détermination des métaux et métalloïdes dans les particules en suspension dans l'air par spectrométrie d'émission atomique avec plasma à couplage inductif - Partie 3 : Analyse. Paris-La-Défense, AFNOR, 2005, 40 p.
- FD ISO 8518 (X 43-102) - Avril 2002 (équivalente à ISO 8518:2001. Décembre 2001). Air des lieux de travail. Dosage du plomb particulaire et des composés particulaires du plomb - Méthode par spectrométrie d'absorption atomique dans la flamme ou méthode par spectrométrie d'absorption avec atomisation électrothermique. Paris-La-Défense, AFNOR, 2002, 38 p.
- NF ISO 30011 Air des lieux de travail. Détermination des métaux et métalloïdes dans les particules en suspension dans l'air par spectrométrie de masse avec plasma à couplage inductif (à publier en 2010)
- A. PELTIER - Utilisation de l'acide fluorhydrique dans les laboratoires de chimie. Cahiers de notes documentaires, 2000, 178, ND 2122, pp. 37-41.
- DEMANGE M., ELCABACHE J.-M. et BOULET A. Mise en solution à froid des membranes en ester de cellulose dans le cadre de l’analyse des aérosols, Canadian Journal of Analytical Sciences and Spectroscopy, 2003, Volume 48, No. 6, pp 362-371.
Historique
| Version | Date | Modification(s) faisant l’objet | Paragraphes |
|---|---|---|---|
| 113/V01.01 | 30/06/2010 | Création |
|
|
| 2012 | Révision de la terminologie | Tous |
| M-124/V01 | Décembre 2015 | Mise en ligne Substances multiples Prélèvement sur cassette Analyse simultanée par ICP/AES |
Date de mise à jour : décembre 2015
Ancien numéro de fiche MétroPol : 113
