Pathologie - Toxicologie
-
Toxicocinétique - Métabolisme [2, 9]
Chez l’animal, le 1,1-dichloro-1-fluoroéthane est principalement absorbé par voie inhalatoire et à un moindre degré par voie digestive. Il est faiblement métabolisé par le foie et excrété via les urines sous forme de métabolites.
Chez l'animal
Le 1,1-dichloro-1-fluoroéthane est facilement et rapidement absorbé par voie respiratoire chez l’animal ; le taux d’absorption est d’environ 40 fois supérieur à celui de la voie orale [8]. Chez le rat (1000 à 14 800 ppm, 6 h), l’absorption se fait en deux phases : la première, rapide (env. 80 min), est attribuée à l’absorption et la mise à l’équilibre du 1,1-dichloro-1-fluoroéthane ; elle est suivie d’une phase linéaire plus lente, liée au métabolisme saturable et au dépôt dans les tissus adipeux avec libération progressive dans le sang.
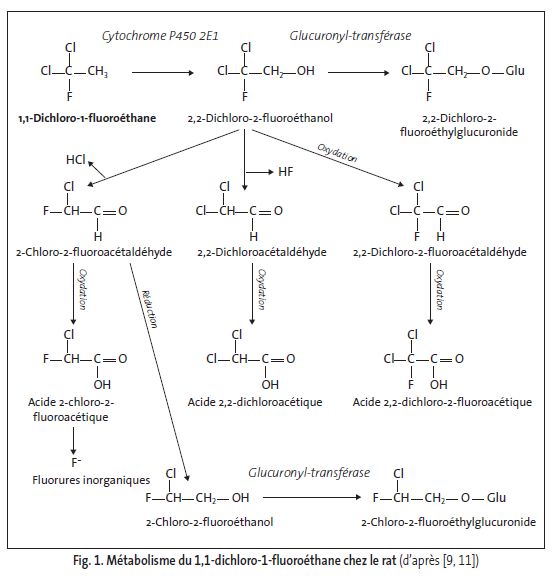
Le taux de transformation du 1,1-dichloro-1-fluoroéthane est faible chez le rat. Le métabolisme passe par une oxydation en présence de cytochrome P450 (voir fig. 1 page suivante).
In vitro, en incubation avec des microsomes hépatiques de rat, le taux de transformation par perte d’halogène est faible (env. 1 %). En présence de microsomes induits par la pyridine, le 1,1-dichloro-1-fluoroéthane subit une oxydation catalysée par le cytochrome P450 2E1 en 2,2-dichloro-2-fluoroéthanol ; en absence d’induction par la pyridine, la formation de métabolites n’est pas quantifiable.
In vivo, il n’y a ni élimination de fluorures urinaires (rat, 0-20 000 ppm, 90j ou 2 ans) ni fixation covalente de métabolites fluorés aux protéines hépatiques (rat, 11 400 ppm, 2 h). Une élimination urinaire de 2,2-dichloro-2-fluoroéthanolglucuronide a été montrée chez le rat (20 000 ppm, 90 j). Le 2,2-dichloro-2-fluoroéthanol libre et l’acide 2,2- dichloro-2-fluoroéthanolglucuronide n’ont pas été détectés à cette concentration d’exposition ; cependant, ce dernier a été décelé dans l’urine de rats exposés pendant 4 h à 40 000 ppm. On peut en conclure l’existence d’un seuil de concentration pour l’oxydation du 2,2-dichloro- 2-fluoroéthanol. Le cytochrome P450 2E1, qui joue un rôle important dans l’oxydation, est présent dans le foie du rat et de l’homme et dans les reins du rat ; sa concentration hépatique est influencée par de nombreux inducteurs comme les solvants organiques et l’éthanol, ce qui entraîne une différence de métabolisme interindividuelle.
Une relation linéaire a été montrée, chez le rat, entre la concentration d’exposition au 1,1-dichloro-1-fluoroéthane et la quantité de 2,2-dichloro-2-fluoroéthanol excrétée dans l’urine. Les autres métabolites excrétés sont : le 2-chloro-2-fluoroéthylglucuronide, le 2-chloro- 2-fluométhanol, l’acide 2-chloro-2-fluoroacétique et des fluorures inorganiques en faibles quantités. Le 1,1-dichloro-1-fluoroéthane inchangé n’est pas détecté [11].
Les acides carboxyliques halogénés se fixent fortement aux protéines plasmatiques ; ils sont lentement éliminés du sang et s’accumulent jusqu'à des concentrations toxiques pour le foie et les testicules.
Aucune donnée n’est disponible sur l’absorption, la distribution, la transformation métabolique ou l’élimination du 1,1-dichloro-1-fluoroéthane chez l’homme.
Schéma métabolique
-
Toxicité expérimentale
-
Toxicité sur l’Homme [14, 15]
